Desvelado el origen de la misteriosa periodicidad del genoma
Cuando se secuenció el genoma humano y el de otros animales, los científicos notaron una marcada periodicidad en el ADN: por cada 10 pares de bases se produce una mayor proporción de los de adenina-timina. Investigadores del IRB Barcelona han descubierto que la estructura que adopta el ADN cuando se empaqueta es la que está detrás de este misterio.
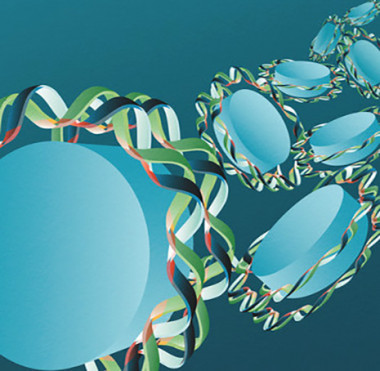
La molécula de ADN, formada por una doble hélice, rodea dos veces las histonas (un tipo de proteínas, coloreadas aquí de azul) formando los nucleosomas (la estructura de compactación más sencilla del ADN). Las zonas rosadas son las que están enriquecidas por pares de bases de adenina-timina. / Iris Joval Granollers
Científicos del Instituto de Investigación Biomédica (IRB Barcelona) presentan una explicación sobre cómo se ha creado a lo largo de la evolución una periodicidad en la secuencia del genoma de todos los eucariotas, desde las levaduras hasta los seres humanos. Los resultados, publicados en la revista Cell, aportan una explicación alternativa a la asumida hasta el momento por la comunidad internacional y basada en la selección natural.
Los investigadores demuestran que los procesos de daño y reparación en el ADN pueden tener un rol en la generación de la periodicidad de secuencia en los genomas. Estos procesos se ven influenciados por la orientación de la estructura del ADN cuando queda empaquetado dentro del núcleo celular y este hecho, a su vez, favorece una determinada composición, de carácter periódico, en los genomas de los eucariotas.
La 'misteriosa' periodicidad del genoma"
La respuesta que damos ayuda a entender mejor porque nuestro genoma y el de otras especies es tal y como lo vemos hoy en día", afirma Núria López-Bigas, responsable del estudio y jefe del laboratorio de Genómica Biomédica en el IRB Barcelona.
Desde que a principios del siglo XXI se dispuso de la secuencia del genoma humano y de otros genomas, como del ratón o la mosca del vinagre, algunos investigadores se dieron cuenta de la marcada periodicidad en la proporción de pares de bases de adeninas (A) y timinas (T). Los científicos observaron que cada 10 pares de bases, la proporción de parejas de A/T era mayor.
Esta periodicidad se ha asociado a cómo el ADN se envuelve alrededor de los nucleosomas (la estructura de compactación más sencilla del ADN, en la que se encuentra rodeando unas proteínas llamadas histonas). La razón esgrimida era que la selección natural favorecía la aparición de las bases de A/T, debido a que proporcionan una mayor flexibilidad a la estructura del ADN, lo que facilita que se pueda doblar como lo hace alrededor de las histonas, formando los nucleosomas.
Las mutaciones de los tumores apuntan la respuesta
Estudiando la distribución de las mutaciones en más de 3.000 tumores humanos, el equipo del IRB Barcelona observó que se acumulan también con una periodicidad de 10 pares de bases en el ADN.
"Investigando cómo se distribuyen las mutaciones de tumores a lo largo del genoma en lugares donde descartamos presencia de selección, vemos una periodicidad de 10 pares de bases muy marcada en el ADN que forma parte de los nucleosomas", explica Oriol Pich, estudiante de doctorado del IRB Barcelona con una beca del Barcelona Institute of Science and Technology (BIST) y primer autor del artículo.
A continuación, estudiaron las mutaciones que se heredan de una generación a otra tanto de humanos como de plantas, y se dieron cuenta de que estas mutaciones heredadas también se acumulan con una periodicidad de 10 pares de bases.Esto ocurre porque la forma en que el ADN se empaqueta en el nucleosoma favorece que haya zonas más o menos propensas a recibir daño y a repararlo, y como resultado son más o menos propensas a recibir mutaciones.
Con este nuevo descubrimiento sobre la influencia de los nucleosomas sobre cómo se generan las mutaciones en el ADN, el equipo dedujo que este hecho podría explicar la creación de la misteriosa periodicidad del genoma de los eucariotas.
Las mutaciones durante millones de años de evolución
Los autores razonaron que como la mayoría de mutaciones que recibimos son citosinas (C) que se convierten en timinas (T), aquellas regiones más propensas a recibir mutaciones a lo largo de millones de años se han ido convirtiendo en parejas de bases A/T en mayor proporción.
Para comprobar este razonamiento, los científicos han hecho una simulación matemática de la evolución del genoma y han demostrado que, efectivamente, la periodicidad del genoma humano y de los otros eucariotas se podría haber formado por esta periodicidad en la tasa de mutaciones.
"Dar esta explicación alternativa a la generación de la periodicidad en la comunidad científica es muy satisfactorio", coinciden Pich y López-Bigas, que ponen en valor este estudio: "Es un conocimiento básico fruto de una investigación guiada por la curiosidad que nos permite comprender mejor lo que observamos en la naturaleza".
Sin embargo, esta investigación no es sólo un avance sobre lo que conocemos de nuestro genoma, sino que también permite entender los procesos por los cuales los tumores adquieren mutaciones. Esto tiene una implicación en encontrar qué mutaciones son relevantes para la génesis de los tumores, otro área en la que el grupo de López-Bigas es experto.
El estudio ha sido posible gracias a la financiación del Consejo Europeo de Investigación (ERC en sus siglas en inglés) a través de un proyecto Consolidator grant a Núria López-Bigas, del Ministerio de Ciencia, a través de fondos FEDER, y de la Generalitat de Catalunya.