La estrategia de los insectos para no congelarse que ayudó a revelar una científica argentina
 SCIENCE PHOTO LIBRARY
SCIENCE PHOTO LIBRARY
Los insectos no tienen capas de pelo para protegerse del frío como otros animales .
Pero tienen algo igualmente efectivo: proteínas anticongelantes.
La existencia de estas proteínas, que evitan que el hielo se forme y esparza en el cuerpo de los insectos, se conocía desde hace décadas. Pero no se sabía como funcionaban.
Un nuevo estudio de la Universidad de Utah y la Universidad de San Diego en Estados Unidos reveló cómo actúan estas proteínas que podrían tener aplicaciones en áreas que van desde la medicina hasta el diseño de aviones.
Estrategias de los insectos
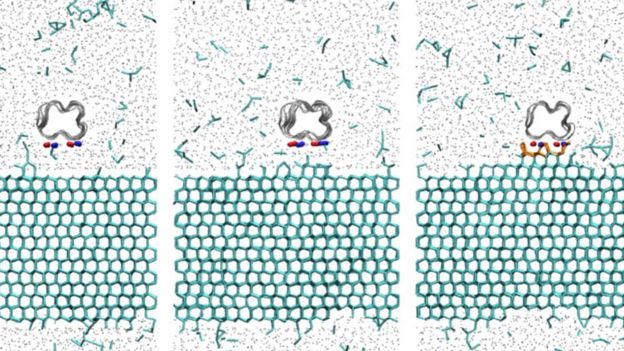
"Como los insectos no pueden controlar su temperatura corporal, usan dos estrategias para evitar la formación de hielo", le dijo a BBC Mundo la científica argentina Valeria Molinero, profesora de química de la Universidad de Utah y una de las autoras del nuevo estudio publicado en la revista de la Academia de Ciencias de Estados Unidos, Proceedings of the National Academy of Sciences.
 PNAS
PNAS
"Una estrategia es la producción de azúcares para formar mezclas muy viscosas que no pueden formar hielo, sino que forman vidrios".
Deshidratarse y producir azúcares para vitrificarse es un mecanismo de hibernación, explicó Molinero.
"La otra estrategia es la producción de proteínas que se pegan a los cristalinos de hielo cuando son pequeños y no los dejan crecer".
Escarabajo
La existencia de proteínas anticongelantes en insectos y otros organismos (por ejemplo, en peces de zonas polares) se conoce desde hace décadas, aunque nuevas proteínas anticongelantes se siguen descubriendo en nuevos organismos, señaló la científica.
"Sin embargo, era un misterio cómo estas proteínas reconocían el hielo, ya que las interacciones moleculares con el agua y el hielo son muy parecidas".
"Se había propuesto que, para reconocer el hielo, las proteínas anticongelantes de insectos organizaban el agua alrededor de ellas en solución para que adopte una estructura como la del hielo. Y que luego el hielo alrededor de la proteína se pegaba al hielo, y así se reconocían".
Sin embargo, según Molinero, esta hipótesis nunca se había testado.
La científica argentina y su estudiante de doctorado, Arpa Hudait, usaron modelos computacionales que representan las proteínas, el agua y el hielo con resolución molecular.
Y su estudio se centró en las proteínas anticongelantes del escarabajo gusano de la harina, Tenebrio molitor.
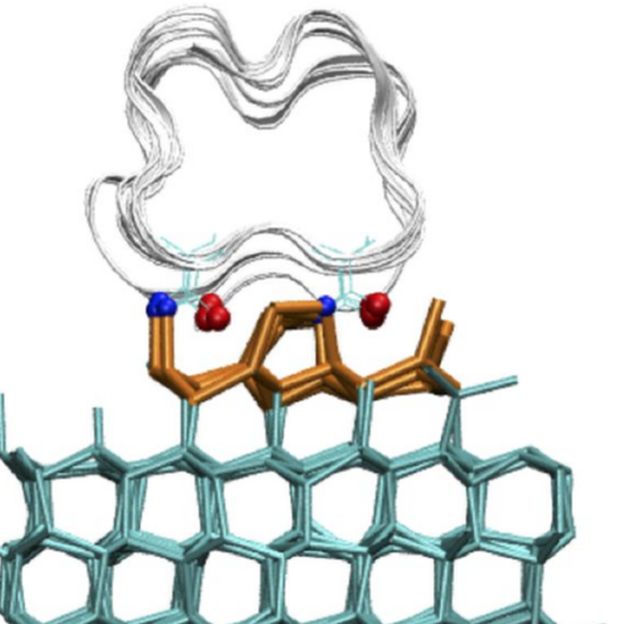
"Investigamos cómo es que la proteína reconoce y se pega al hielo. Lo que encontramos es que la proteína no necesita organizar el agua antes de pegarse. Es suficiente con que la proteína se posicione sobre el hielo en la configuración adecuada, y luego se pega muy rápido".
"Como un almohadón"
Molinero explicó que las proteínas anticongelantes "se pegan fuertemente al hielo. Eso hace que cuando la temperatura baja y el hielo quiere crecer, la superficie de los cristales desarrolla curvatura -como un almohadón al que se le colocan encima piedras que se hunden- formando una superficie curva".
 PNAS
PNAS
"Eso hace que el hielo tenga más superficie expuesta al agua líquida que lo que tendría si la superficie fuera plana. Ese exceso de interfaz entre agua y hielo desestabiliza a los cristales, impidiéndoles crecer".
Esto permite de acuerdo a la investigadora que los insectos puedan vivir sin que toda el agua en su organismo se congele, aunque pueden tener pequeños cristalinos de hielo, lo que no sería letal.
Simulaciones
La especialidad de Molinera, quien vive desde hace casi 18 años en Estados Unidos, es la química física computacional y la simulación de hielo a diferentes escalas.
"En las simulaciones moleculares los científicos hacen el experimento en forma virtual, en computadoras", explicó la investigadora a BBC Mundo.
 SCIENCE PHOTO LIBRARY
SCIENCE PHOTO LIBRARY
"Se construye un modelo de las moléculas, en ese caso, las proteínas y el agua. El modelo indica cual es la fuerza de atracción y repulsión entre cada átomo de las moléculas en función de la distancia entre las moléculas", dijo.
"Los programas de simulación molecular usan esas fuerzas para mover las moléculas, usando relaciones entre fuerza y aceleración (mecánica newtoniana)".
"Usando esas relaciones, la computadora predice cómo las moléculas se mueven, y esa trayectoria de todas las moléculas en función del tiempo es lo que nosotros analizamos para entender el mecanismo molecular".
Medicina y aviones
Pero ¿por qué es importante copiar algún día el mecanismo de las proteínas anticongelantes?
Futuras aplicaciones en diversas áreas podrían incluir desde la preservación de órganos para trasplantes hasta el diseño de alas de aviones libres de hielo.
 GETTY IMAGES
GETTY IMAGES
"La importancia de nuestro descubrimiento es que nos permite entender qué elementos son importantes para diseñar moléculas sintéticas que cumplan la misma función que las proteínas anticongelantes pero se puedan optimizar -en costo y función- para aplicaciones especificas", afirmó Molinero.
"Existe un mercado potencial para anticongelantes basado en el mismo mecanismo, pero si no se comprende el mecanismo, es difícil definir y optimizar las moléculas", concluyó.
No hay comentarios:
Publicar un comentario